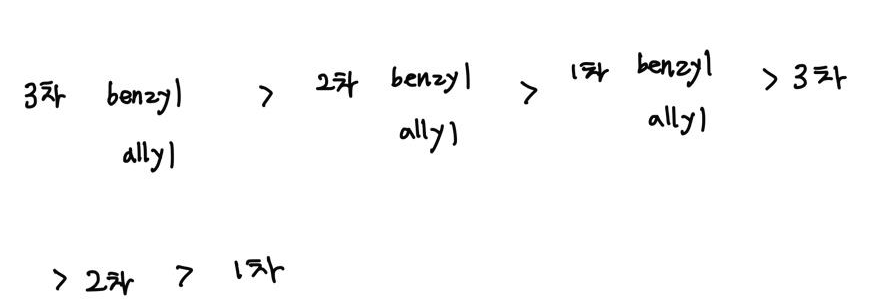오늘은 탄소 라디칼 안정도와 관련 반응에 대해 알아보겠습니다.
두 물체 간 C - H 결합 해리 에너지 ( 일명 BDE )를 비교할 때 탄소 라디칼 안정도를 비교하고는 합니다.
( 탄소의 혼성이 같다는 전제가 필요합니다.)
결합이 균일 결합 분해 방식으로 해제된다면 라디칼을 형성합니다.
탄소 라디칼은 sp2 혼성을 하고, 비공유 전자는 p 오비탈에 배치되며 거의 평면 구조에 가깝습니다.
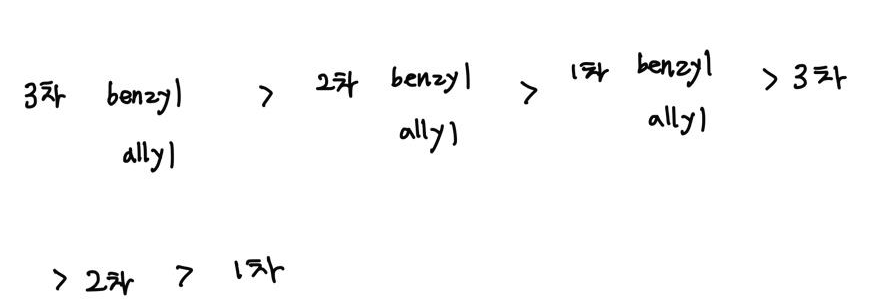
벤질, 알릴은 공명 + 유도 효과로 인해 더욱 안정한 탄소 라디칼을 형성합니다.
BDE가 낮은 C-H, 가장 약한 C-H는 균일 분해 시 안정한 탄소 라디칼 구조를 형성한다는 것을 의미합니다.
( 바이닐 라디칼은 공명되지 않기 때문에 매우 불안정합니다.)
라디칼 반응은 자외선 (hv) or 300 도 이상의 고열이 필요합니다.
아니면 ROOR, AIBN과 같은 개시제가 있어야 반응을 시작할 수 있습니다.
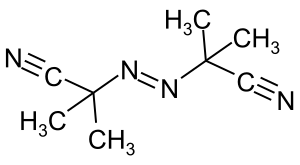 AIBN
AIBN
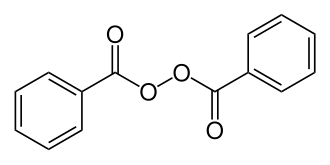 ROOR 중 하나인 (PhCO2)2
ROOR 중 하나인 (PhCO2)2
벤조일 퍼옥사이드는 O-O 결합이 약해서 개시제로 많이 사용된다.
탄소 라디칼 안정도에 대해 알아보았습니다.
탄소 라디칼이 무엇인지, 그것의 안정도에 대해 알아보았지요.
탄소 라디칼 경유 반응들에 대해 알아보겠습니다.
라디칼을 경유하는 반응으로는
1. Alkane의 할로젠 치환 반응
2. 알릴 자리 Br 치환 반응
3. 알켄에 HBr 첨가
가 있습니다.
1. 알케인의 할로젠화 치환 반응
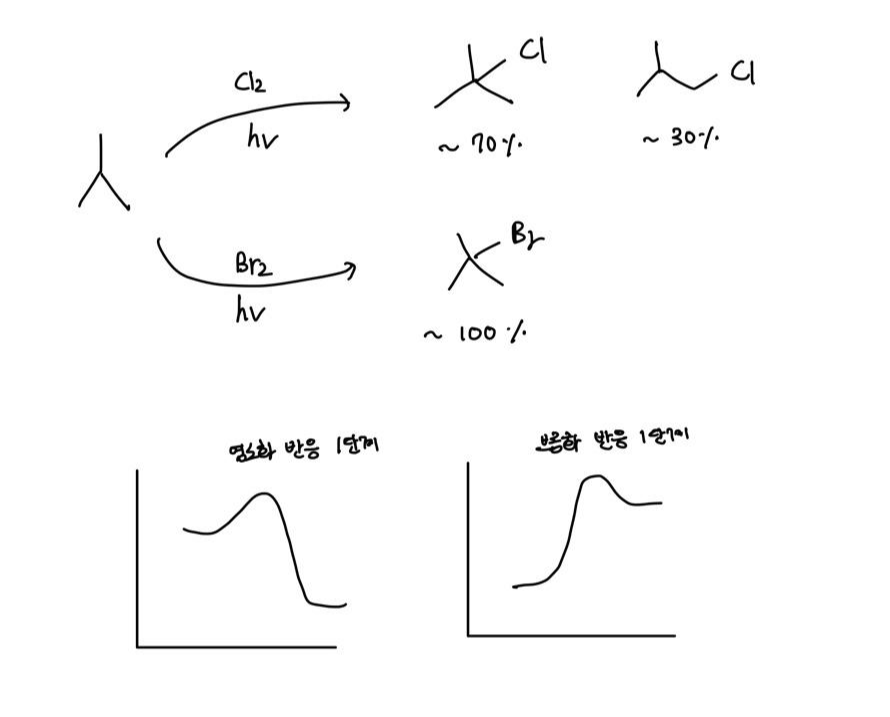
염소화 반응은 RDS가 발열 반응입니다.
브롬화 반응은 RDS가 흡열 반응입니다. 따라서 전이 상태는 중간체와 유사하며 라디칼의 특성을 많이 가지기 때문에 기질의 차수에 민감합니다.
선택성 : F2 < CI2 < Br2 < I2
반응성 : F2 > CI2 > Br2 > I2
라디칼 안정성 : F < CI < Br < I
라디칼의 불안정성은 원자핵의 에너지에 의해 생기는 데 크기가 클수록 라디칼 전자가 원자핵으로부터 멀어져 원자핵의 에너지를 덜 받는데요. 따라서 크기가 큰 I, Br, CI, F 순으로 라디칼이 안정합니다.
2. allyl 자리 브로민 라디칼 치환 반응
극성 첨가 반응과 라디칼 치환 반응이 경쟁하는 것을 막기 위해 Br2 대신에 브로민 라디칼을 공급하는 NBS를 주로 사용합니다.

3. 알켄 HBr 첨가 반응

개시제가 균일 분해 후 수소 제거로 Br 라디칼을 만들어 냅니다. Br은 라디칼 첨가 후 생성물을 만들고, 짝지음에 의해 라디칼이 소멸되면 반응이 완결됩니다.
alkene에 HBr이 극성 반응으로 첨가시에는 markovnikov 식으로 첨가가 일어납니다.
하지만, 알켄의 HBr 첨가반응(개시 조건이 갖추어졌을 때)은 anti markovnikov 첨가가 일어납니다. ( 덜 치환된 탄소로 br이 자리잡습니다.)
첨가 반응의 위치 선택성은 더 안정한 중간체를 거치는 방향으로 결정된다고 말할 수 있습니다.
HCI, HI 등으로 반응이 원활하게 진행되지 않기 때문에 HBr을 주로 사용합니다.
지금까지 탄소 라디칼 경유 반응들에 대해 알아보았습니다. 이런 반응들은 크게 치환, 첨가 반응이 있는데요.
substitution reaction에는 알릴 자리 브로민 치환, 알케인의 할로젠화 치환이 있고, addition reaction에는 알켄의 HBr 첨가가 있습니다!
이들을 잘 구분해서 기억해두도록 합시다.