지난 번에는 산도를 결정하는 요인에 대해 알아보았습니다.
오늘은 배운 것을 토대로 PEET 유기화학 기출 문제를 바탕으로 수소의 산도를 비교해 보도록 하겠습니다.
1.
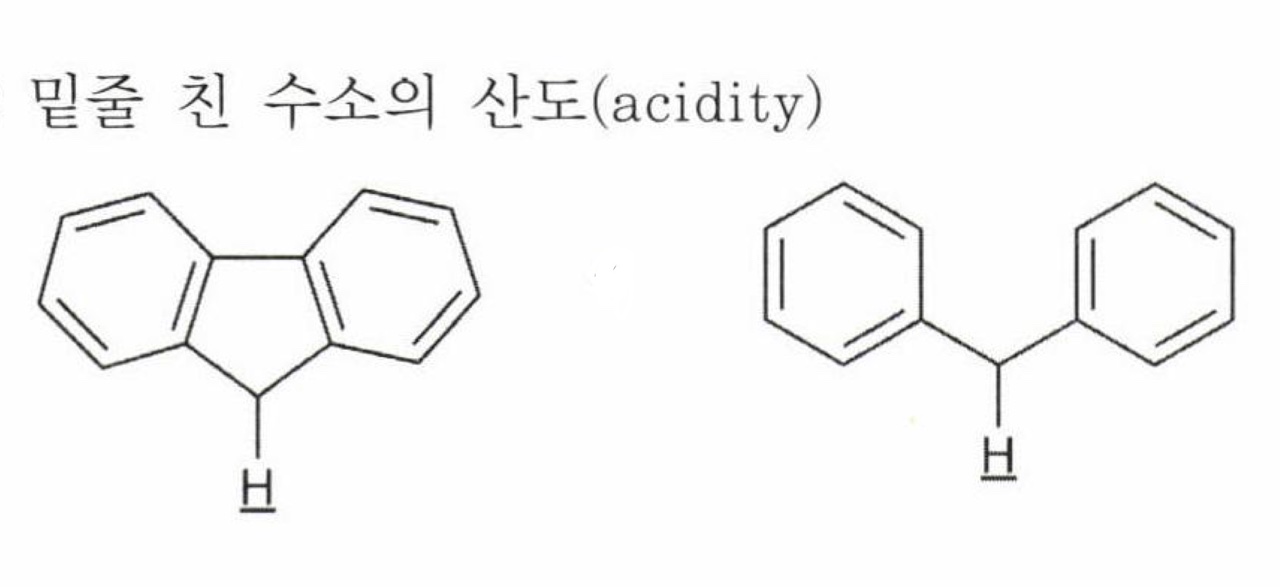
산도는 짝염기의 안정성으로 판단해야 합니다.

짝염기를 그리면 위와 같은 구조가 나오는데요.
왼쪽은 벤젠고리와 가운데 오각고리에 방향족이 만들어지고, 오른쪽은 벤젠고리만 방향족이어서 상대적으로 왼쪽 구조의 짝염기가 더 안정합니다.
참고로 방향족성은 고리, 평면, 컨쥬게이션, (4n + 2) 파이 전자를 만족해야 합니다.
답 : 따라서 왼쪽의 산도가 더 크다고 말할 수 있습니다.
2.
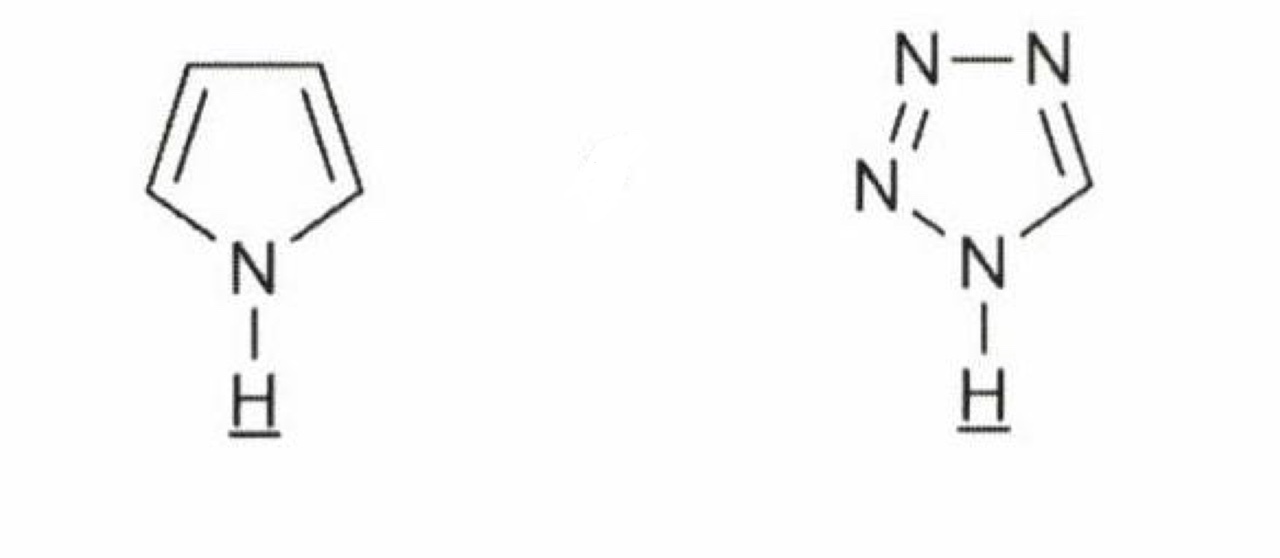
답 : 오른쪽 수소의 산도가 더 큽니다.
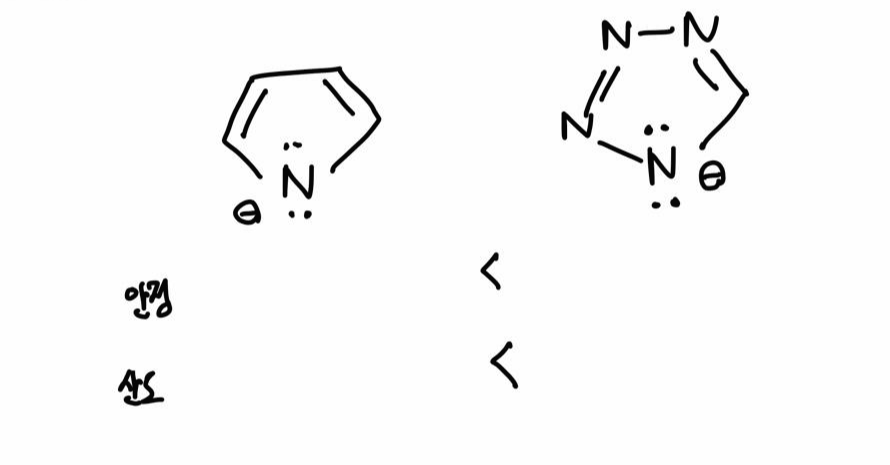
왜냐하면 질소가 탄소보다 유발효과가 더 크기 때문에 상대적으로 짝염기의 음이온을 안정화 시켜줍니다!
3.
다음 구조에서 어느 수소의 산성도가 가장 큰가?
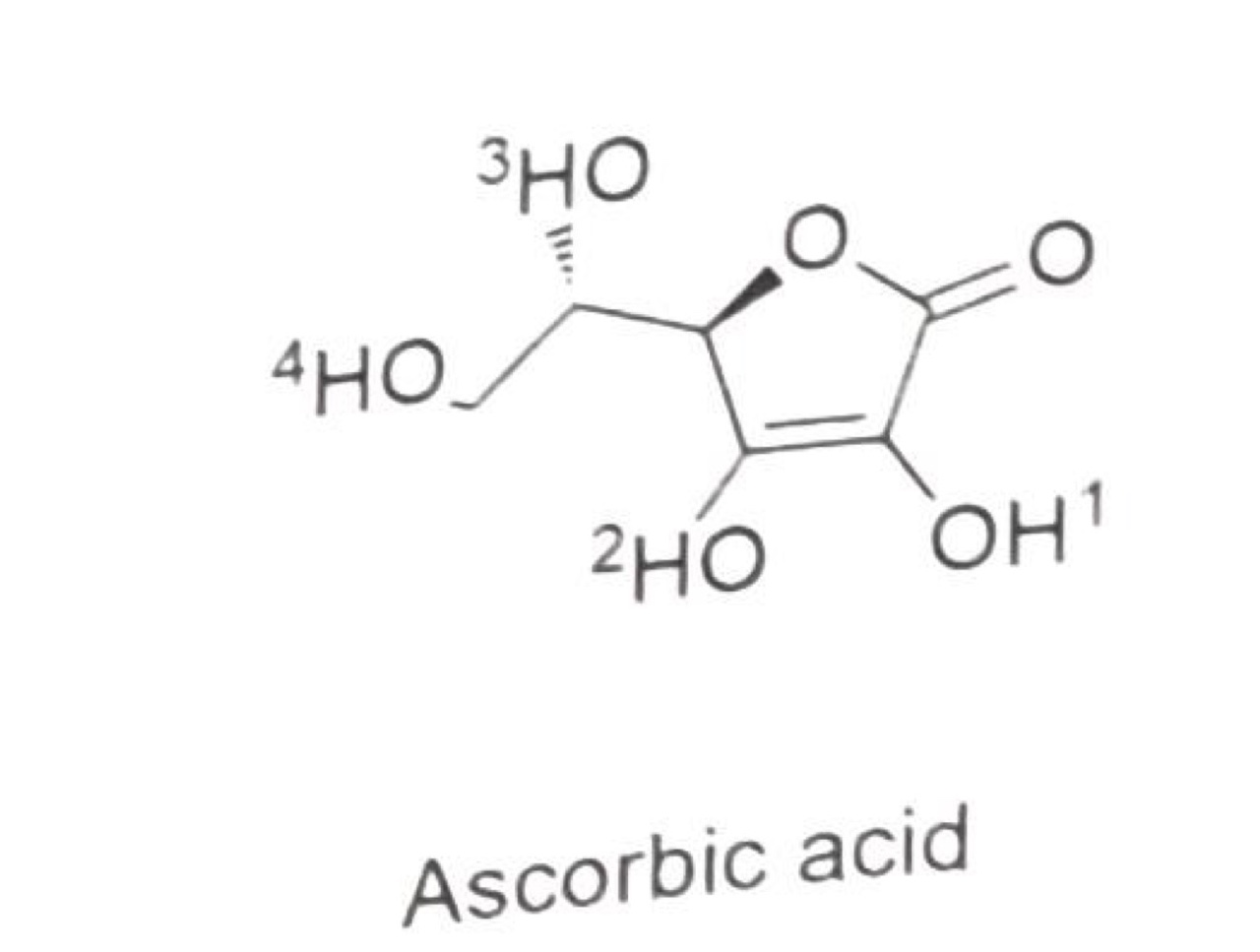
답 : 2번 수소의 산성도가 가장 큽니다.
풀이
3번과 4번은 sp3 탄소에 결합해 있고, 1번 2번은 sp2 탄소에 결합해 있습니다.
따라서 1,2 번이 3,4번 보다 산도가 큽니다.

1번과 2번의 짝염기 공명 구조를 그려 봅시다.
위의 2번 수소를 뗀 짝염기 공명 구조가 1번 수소를 뗀 것보다 음전하가 비편재되는 범위가 크고, 산소에 음전하를 두는 공명 구조가 존재하기 때문에 더 안정합니다.
수소를 잘 내놓는 ( 짝염기가 안정한 ) 것이 산성도가 크다고 말할 수 있지요.
따라서 2번 수소가 위의 구조 중 산성도가 가장 큽니다.
공부해도 공부해도 어렵네요..
산도 비교시에는 짝염기의 공명구조를 잘 그릴 줄 아느냐가 중요한 것 같아요.
지금까지 산성도에 영향을 주는 요소들에 대해 알아보았습니다.
오늘은 염기성도 판단하는 방법에 대해 알아볼 계획입니다.
염기는 양성자 받개, 전자쌍 주개입니다.
따라서 음전하가 편재되어 있고, 음이온이 불안정할 수록 염기도가 증가합니다.
1. 원소효과
같은 주기의 경우 전기음성도가 작을 수록 염기도가 증가합니다.
C- > N - > O - > F-
같은 족의 경우 원자의 크기가 작을 수록 염기도가 증가합니다.
F - > CI - > Br - > l -
2. 공명효과
염기 구조가 공명한다면 전자쌍이 비편재화 되기 때문에 염기도가 감소합니다.
3. 유발효과
전기음성도가 큰 원자가 가까이 있거나 많이 있을 수록 염기가 안정해지기 때문에 염기도가 감소합니다.
4. 혼성화효과
염기의 음전하를 가지고 있는 원자의 혼성화 s 분율이 작을수록 염기도가 증가합니다.

오른쪽은 탄소보다 전기음성도가 큰 산소가 존재하기 때문에 염기가 안정해집니다.
염기는 불안정할 수록 염기도가 증가하므로 왼쪽 구조가 오른쪽 구조보다 염기도가 더 큽니다.
산성도 비교랑 많이 헷갈리죠?
둘을 잘 구별해서 기억해두어야 합니다.
'구조와 반응성' 카테고리의 다른 글
| FC 알킬화 반응 과 한계점 (0) | 2022.04.11 |
|---|---|
| 방향족의 벤질자리 반응 (0) | 2022.04.10 |
| 탄소 라디칼 안정도와 관련 반응 (0) | 2022.04.06 |
| 유기분자들의 물리적 성질( 물성 ) 에 대해 공부해 보자 (0) | 2022.02.27 |
| 각종 물질들 pKa 암기하기 (0) | 2022.02.26 |