반응형
유기화학 치환반응 메커니즘과 입체화학을 공부할려고 합니다.
치환반응에는 Sn2와 Sn1이 있습니다.
SN2 반응(이분자 친핵성 치환반응)
협동으로 한 단계로 일어납니다.
V = K[친핵체][기질]
친핵체가 탄소를 공격함과 동시에 이탈기가 떨어져 나갑니다.
친핵체가 탄소를 후방 공격을 합니다.
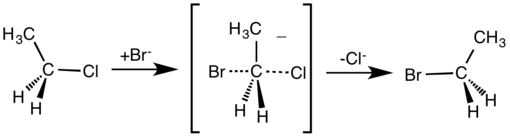
구조가 우산이 뒤집힌 것처럼 반전됩니다.
절대배열은 항상 반전되는 것이 아니고, 이탈기와 친핵체의 RS 배열 1순위 일때 반전됩니다.
Sn1 반응(일분자 친핵성 치환반응)
= 가수분해 반응 ( 용매 분자가 친핵체로 작용한 반응)
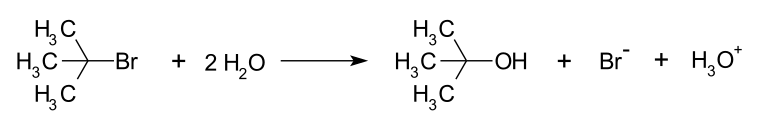
v(속도) =k[기질]
세단계를 거친다.
1. R-X에서 이탈기의 자발적 해리가 일어납니다.
이 때 탄소 양이온이 형성되고, RDS입니다.

2. 친핵체가 탄소 양이온을 공격합니다.

3. 물이 염기로 작용해 탈양성자화 반응이 일어납니다.

알파 탄소만 카이랄 중심이라면 이론적으로는 라세미화가 일어납니다.
다만 실험을 하면 불완전한 라세미화가 일어나는데 반전된 형태가 더 많이 나타납니다.
( 자유탄소양이온 뿐만 아니라 이온쌍이 생겨나기 때문입니다.)
| Sn2 | Sn1 | |
| Nu | 강친핵체 | 약친핵체 선호 |
| 기질 | 메틸, 1차 알킬 할라이드 선호 2차는 느린편 |
2,3차 알킬 할라이드 부터 가능 |
| 용매 | 극성 비양성자성 ( 활성화 에너지 값을 줄임) |
극성 양성자성 (전이 상태 안정화) |
| 이탈기 | F- < CI - < Br - < I - | |
반응형
'할로젠화 알킬' 카테고리의 다른 글
| 이웃자리 효과(NGP) (0) | 2022.05.14 |
|---|---|
| Sn1 반응의 반응성에 대해 알아보자 (0) | 2022.04.15 |
| Sn2 반응의 속도를 결정짓는 요인들에 대해 알아보자 (1) | 2022.04.14 |